Als Lieferant von Triazol erhalte ich häufig Anfragen zu den Gitterenergien von Triazol-Kristallen. Die Gitterenergie ist eine grundlegende Eigenschaft, die die physikalischen und chemischen Eigenschaften kristalliner Substanzen maßgeblich beeinflusst. In diesem Blog werden wir uns mit dem Konzept der Gitterenergie befassen, die Faktoren untersuchen, die die Gitterenergien von Triazolkristallen beeinflussen, und seine praktischen Auswirkungen verstehen.
Gitterenergie verstehen
Gitterenergie ist definiert als die Energie, die freigesetzt wird, wenn ein Mol einer ionischen Verbindung aus ihren konstituierenden Ionen im gasförmigen Zustand gebildet wird. Obwohl die Bindung bei kovalenten Verbindungen wie Triazol nicht rein ionisch ist, kann ein ähnliches Konzept zur Beschreibung der mit der Bildung des Kristallgitters verbundenen Energie angewendet werden. Es stellt die Stärke der Kräfte dar, die die Moleküle im Festkörpergitter zusammenhalten.
Die Gitterenergie kann mit theoretischen Modellen wie dem Born-Haber-Zyklus berechnet oder durch rechnerische Methoden abgeschätzt werden. Der Born-Haber-Zyklus ist ein thermochemischer Zyklus, der die Gitterenergie mit anderen thermodynamischen Größen wie Ionisierungsenergie, Elektronenaffinität und Bildungsenthalpie in Beziehung setzt. Für komplexe organische Verbindungen wie Triazol sind jedoch quantenmechanische Berechnungsmethoden oft besser geeignet.
Faktoren, die die Gitterenergien von Triazolkristallen beeinflussen
Molekulare Struktur
Die Struktur von Triazolmolekülen spielt eine entscheidende Rolle bei der Bestimmung der Gitterenergie. Triazol liegt in verschiedenen isomeren Formen vor, beispielsweise als 1,2,3-Triazol und 1,2,4-Triazol. Diese Isomere haben unterschiedliche Molekülgeometrien, die zu Variationen in den zwischenmolekularen Kräften und Packungsanordnungen im Kristallgitter führen.
Beispielsweise kann die Ausrichtung der Stickstoffatome im Triazolring die Dipol-Dipol-Wechselwirkungen zwischen Molekülen beeinflussen. Wenn die Dipolmomente benachbarter Moleküle günstig ausgerichtet sind, werden die zwischenmolekularen Kräfte stärker, was zu einer höheren Gitterenergie führt. Darüber hinaus kann das Vorhandensein von Substituenten am Triazolring auch die Molekülstruktur und die intermolekularen Wechselwirkungen verändern. Substituenten unterschiedlicher Größe, Elektronegativität und sterischer Wirkung können die Gitterenergie entweder erhöhen oder schwächen.
Intermolekulare Kräfte
Intermolekulare Kräfte sind Anziehungs- oder Abstoßungskräfte zwischen Molekülen. In Triazolkristallen wirken verschiedene Arten intermolekularer Kräfte, darunter Wasserstoffbrückenbindungen, Dipol-Dipol-Wechselwirkungen und Van-der-Waals-Kräfte.
Wasserstoffbrückenbindungen sind eine besonders starke intermolekulare Kraft, die die Gitterenergie deutlich erhöhen kann. Triazolmoleküle können über die Stickstoffatome im Ring und alle wasserstofftragenden Substituenten Wasserstoffbrückenbindungen bilden. Wenn ein Triazol-Derivat beispielsweise eine Hydroxylgruppe (-OH) oder eine Aminogruppe (-NH₂) aufweist, können sich zwischen diesen Gruppen und den Stickstoffatomen benachbarter Triazol-Moleküle Wasserstoffbrückenbindungen bilden.
Dipol-Dipol-Wechselwirkungen treten zwischen polaren Molekülen auf. Triazol hat aufgrund des Elektronegativitätsunterschieds zwischen Stickstoff- und Kohlenstoffatomen im Ring ein Dipolmoment ungleich Null. Diese Dipol-Dipol-Wechselwirkungen tragen zur Stabilität des Kristallgitters bei. Van-der-Waals-Kräfte, zu denen auch die Londoner Dispersionskräfte gehören, sind in allen Molekülen vorhanden und entstehen durch vorübergehende Schwankungen der Elektronendichte. Obwohl Van-der-Waals-Kräfte im Vergleich zu Wasserstoffbrückenbindungen und Dipol-Dipol-Wechselwirkungen relativ schwach sind, können sie dennoch einen Einfluss auf die Gitterenergie haben, insbesondere bei unpolaren oder schwach polaren Triazol-Derivaten.
Kristallverpackung
Auch die Art und Weise, wie sich Triazolmoleküle im Kristallgitter anordnen, beeinflusst die Gitterenergie. Effiziente Packungsanordnungen, bei denen Moleküle eng zusammengepackt sind, führen zu stärkeren intermolekularen Wechselwirkungen und höheren Gitterenergien. Die Kristallpackung wird durch die Molekülform, -größe und die Art der zwischenmolekularen Kräfte beeinflusst.
Wenn beispielsweise Triazol-Moleküle eine regelmäßige und symmetrische Form haben, können sie sich effizienter im Kristallgitter verpacken als Moleküle mit unregelmäßiger Form. Darüber hinaus kann das Vorhandensein intermolekularer Kräfte die Packungsanordnung steuern. Wasserstoffbrücken beispielsweise können die relative Ausrichtung von Molekülen im Gitter bestimmen und so zu einer geordneteren und stabileren Struktur führen.
Praktische Implikationen von Gitterenergien in Triazolkristallen
Löslichkeit
Die Gitterenergie von Triazolkristallen hängt von ihrer Löslichkeit in verschiedenen Lösungsmitteln ab. Verbindungen mit hohen Gitterenergien sind in Lösungsmitteln im Allgemeinen weniger löslich, da mehr Energie erforderlich ist, um die intermolekularen Kräfte im Kristallgitter aufzubrechen und die Moleküle im Lösungsmittel zu dispergieren.
Wenn ein Triazol-Derivat starke Wasserstoffbrückenbindungen und eine hohe Gitterenergie aufweist, ist es in unpolaren Lösungsmitteln weniger löslich. Wenn andererseits die intermolekularen Kräfte relativ schwach sind, kann die Verbindung in einem größeren Spektrum an Lösungsmitteln besser löslich sein. Das Verständnis der Gitterenergie kann bei der Auswahl geeigneter Lösungsmittel für die Reinigung und Formulierung von Produkten auf Triazolbasis hilfreich sein.
Stabilität
Die Gitterenergie beeinflusst auch die Stabilität von Triazolkristallen. Verbindungen mit hohen Gitterenergien sind stabiler, da die intermolekularen Kräfte, die die Moleküle zusammenhalten, stärker sind. Dies bedeutet, dass es unter normalen Bedingungen weniger wahrscheinlich ist, dass sie Phasenübergänge durchlaufen oder sich zersetzen.
Bei pharmazeutischen Anwendungen ist die Stabilität triazolhaltiger Arzneimittel entscheidend für deren Haltbarkeit und Wirksamkeit. Bei einem Arzneimittel mit einem hochenergetischen Kristallgitter ist es wahrscheinlicher, dass es seine chemische Integrität im Laufe der Zeit beibehält, was das Risiko eines Abbaus verringert und eine konsistente therapeutische Wirkung gewährleistet.
Reaktivität
Die Gitterenergie kann die Reaktivität von Triazolkristallen beeinflussen. In manchen Fällen kann eine hohe Gitterenergie die Beweglichkeit von Molekülen im Festkörper einschränken und so das Ablaufen chemischer Reaktionen erschweren. Unter bestimmten Bedingungen, beispielsweise bei hoher Temperatur oder in Gegenwart eines Katalysators, kann die Gitterenergie jedoch überwunden werden und die Reaktion kann ablaufen.
Beispielsweise kann in der organischen Synthese die Reaktivität von Triazol-Derivaten durch Modifizierung der Gitterenergie durch Änderungen in der Molekülstruktur oder der Kristallpackung eingestellt werden. Dies kann zur Steuerung der Reaktionsgeschwindigkeit und Selektivität nützlich sein.
Verwandte Verbindungen und ihre Bedeutung
In unserem Portfolio als Triazol-Lieferant bieten wir auch verwandte Verbindungen an, die in der pharmazeutischen und chemischen Industrie von Bedeutung sind. Zum Beispiel,6 - Fluorindol - 3 - Carboxaldehydist ein wertvolles pharmazeutisches Zwischenprodukt. Es wird bei der Synthese verschiedener biologisch aktiver Verbindungen verwendet und seine Eigenschaften werden auch von Faktoren beeinflusst, die denen von Triazolkristallen ähneln, wie z. B. intermolekularen Kräften und Kristallpackung.

Eine weitere Verbindung,1 - Methyl-3-(trifluormethyl)-1H-pyrazol-4-carbonsäureist auch ein wichtiger Baustein in der organischen Synthese. Das Vorhandensein der Trifluormethylgruppe in dieser Verbindung kann ihre intermolekularen Wechselwirkungen und Gitterenergie beeinflussen, was wiederum Auswirkungen auf ihre Löslichkeit, Stabilität und Reaktivität hat.
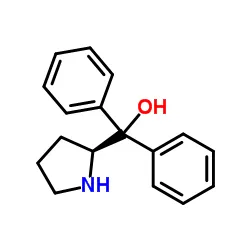
2 - Pyrrolidinmethanol, A,a - Diphenyl -, (2S) -ist eine chirale Verbindung, die in der asymmetrischen Synthese Anwendung findet. Die Gitterenergie seiner Kristalle kann seine physikalischen und chemischen Eigenschaften wie Schmelzpunkt und Löslichkeit beeinflussen, die wichtige Faktoren bei Synthese- und Reinigungsprozessen sind.
Abschluss
Die Gitterenergie von Triazolkristallen ist eine komplexe Eigenschaft, die von der Molekülstruktur, zwischenmolekularen Kräften und der Kristallpackung beeinflusst wird. Das Verständnis der Gitterenergie hat praktische Auswirkungen auf verschiedene Bereiche, darunter Löslichkeit, Stabilität und Reaktivität. Als Triazol-Lieferant sind wir bestrebt, qualitativ hochwertige Triazol-Produkte und verwandte Verbindungen bereitzustellen. Unser Wissen über die Gitterenergie und ihre Auswirkungen auf die Eigenschaften dieser Verbindungen ermöglicht es uns, Produkte anzubieten, die den spezifischen Bedürfnissen unserer Kunden entsprechen.
Wenn Sie am Kauf von Triazol oder verwandten Verbindungen interessiert sind oder Fragen zu deren Eigenschaften und Anwendungen haben, laden wir Sie ein, uns für weitere Gespräche und Beschaffungsverhandlungen zu kontaktieren. Wir freuen uns darauf, mit Ihnen zusammenzuarbeiten, um Ihre chemischen Anforderungen zu erfüllen.
Referenzen
- Atkins, PW, & de Paula, J. (2014). Physikalische Chemie. Oxford University Press.
- McMurry, J. (2012). Organische Chemie. Engagieren Sie das Lernen.
- Huheey, JE, Keiter, EA und Keiter, RL (1993). Anorganische Chemie: Prinzipien der Struktur und Reaktivität. HarperCollins College Publishers.




